Une technologie innovante
pour traiter des maladies graves
Une administration dans la bouche pour délivrer des actifs pharmaceutiques dans toutes les cellules : ARN interférents, ions métalliques, peptides…Medesis Pharma ouvre le champs des possibles !
Maladie d’Alzheimer
La maladie d’Alzheimer (AD) est une affection neurodégénérative progressive caractérisée par la présence de plaques extracellulaires d’amyloïde beta (Aβ) et de réseaux intracellulaires de neurofibrilles. Cette maladie est la plus fréquente et la plus invalidante cause de démence dans la population âgée. Elle concerne 50 millions de personnes au niveau mondial et est en constante progression dans de nombreux pays du fait de l’augmentation de l’espérance de vie. Il n’existe à l’heure actuelle aucun traitement pour cette maladie.
Nanolithium (NP03) pour le traitement de la maladie d'Alzheimer
Des études précliniques ont été réalisées sur un modèle animal de la maladie (rat transgéniques McGill-R-Thy1-APP Alzheimer) pour évaluer l’effet thérapeutique de NP03 en tant que traitement modificateur de la maladie, en collaboration avec l’équipe du Professeur Claudio Cuello (McGill University, Montreal CA). Claudio Cuello est internationalement connu pour ses travaux sur cette maladie et a mis au point ce modèle animal.
Wilson EN, Do Carmo S, Welikovitch LA, Hall H, Aguilar LF, Foret MK, Iulita F, Jia DT, Marks AR, Allard S, Emmerson JT, Ducatenzeiler A, and Cuello C – NP03, a microdose Lithium Formulation, Blunts Early Amyloid Post-Plaque Neuropathology in McGill-R-Thy1-APP Alzheimer-Like Transgenic Rats – J. of Alzheimer’s Disease, 73 (2020) 723-739.
Wilson EN, Do Carmo S, Iulita MF, Hall H, Austin G, Jia D, Malcolm J, Foret M, Marks AR, Butterfield D and Cuello C, – Microdose Lithium NP03 Diminishes Pre-Plaque Oxidative Damage and Neuroinflammation in a Rat model of Alzheimer’s-like Amyloidosis – Current Alzheimer Research, 2018, 15, 1220-1230
Wilson EN, Do Carmo S, Iulita MF, Hall H, Ducatenzeiler A, Marks AR, Allard S, Jia DT, Windheim J and Cuello A; BACE 1 inhibition by microdose lithium formulation NP03 rescues memory loss and early stage amyloid neuropathology – Translational Psychiatry (2017) 7, e1190.
Les résultats ont été les suivants :
NP03 corrige ou retarde les déficits dans divers tests cognitifs et/ou comportementaux, diminue fortement l’expression du peptide amyloïde beta et l’expression du gène BACE1 (impliqué dans sa production) inhibe la GSK-3 β et induit la neurogenèse dans l’hippocampe.
Une phase I a été validée.
Une étude de phase II va débuter au premier trimestre 2022
Maladie de Huntington
La maladie de Huntington est une maladie génétique neurodégénérative progressive fatale
Il n’existe à l’heure actuelle aucun traitement de cette maladie.
MEDESIS PHARMA développe trois futurs médicaments pour traiter la Maladie de Huntington
NanoLithium
Pour prévenir et traiter les troubles psychiatriques (troubles de l’humeur et dépression) et un déclin des capacités cognitives (troubles de la mémoire, de la conversation et de la prise de décision)
Les études précliniques réalisées à l’Université Columbia à Vancouver (publication de l’équipe du Professeur Michael Hayden ) ont montré sur un modèle transgénique YAC128 une amélioration nette des performances motrices et du comportement
Pouladi MA, Brillaud E, Xie Y, Conforti P, Graham RK, Ehrnhoefer DE, Franciosi S, Zhang W, Poucheret P, Compte E, Maurel JC, Zuccato C, Cattaneo E, Néri C, Hayden MR.; NP03, a novel low-dose lithium formulation, is neuroprotective in the YAC128 mouse model of Huntington disease – Neurobiol. Dis. 2012 Dec;48(3):282-9.
Le produit possède une désignation Orphan Drug auprès de l’EMA et de la FDA
NanosiRNA HD
Pour inhiber l’expression du gène muté responsable de la maladie, avec un ARN interférent formulé dans Aonys®.
Il est ainsi possible de cibler spécifiquement les ARNm mutants avec un ARNi allèle-spécifique dirigé contre les SNP.
La technologie de drug delivery développée par MEDESIS PHARMA permet d’administrer par voie buccale des siRNA non modifiés en les transportant dans des lipoprotéines HDL qui se structurent à la traversée de la muqueuse buccale, et de les délivrer intacts dans toutes les cellules, en particulier dans les neurones et les astrocytes avec un passage de la Barrière Hémato Encéphalique.
Le plan de développement a été validé par l’EMA (Agence Européenne du médicament) en mai 2021.
NanoPEP42
Pour empêcher la mort neuronale en bloquant l’agrégation de la huntingtine mutée intracellulaire avec un peptide isolé dans la Huntingtine et formulé dans Aonys®
Le peptide P42 a été identifié dans l’équipe de Florence Maschat (CNRS, Institut de Génomique Fonctionnelle Montpellier)
P42, un peptide 23aa isolé de Htt endogène dans une région riche en sites protéolytiques qui joue un rôle critique dans le processus de pathogenèse. Nous avons montré qu’il empêchait les phénotypes pathologiques induits par mHtt. La neuroprotection induite par P42 a d’abord été démontrée à l’aide d’un modèle de Drosophile de HD sur l’agrégation mHtt, sur différents phénotypes neuronaux induits par polyQ-hHtt, y compris la dégénérescence oculaire ou l’altération du trafic axonal vésiculaire, et sur des comportements physiologiques tels que la locomotion larvaire et la survie des adultes.
Le potentiel thérapeutique de P42 a ensuite été confirmé dans un modèle murin de la maladie, la souris R6/2, en utilisant la microémulsion Aonys® permettant une administration non invasive par muqueuse buccale/rectale, P42 a été efficacement délivrée dans le cerveau et a ciblé la plupart des cellules, y compris les neurones striataux. Il a permis une nette amélioration des troubles comportementaux associés à la MH tels que la saisie des pieds, la latence de chute, le test du rotarod et le poids corporel, ainsi que plusieurs marqueurs histologiques de la MH sur des coupes cérébrales tels que l’agrégation, l’astrogliose ou l’élargissement des zones ventriculaires.
Plus récemment, nous avons rapporté le mécanisme d’action de P42 sur la voie BDNF/TrkB chez les souris R6/2. L’expression du BDNF est fortement réduite chez les souris R6/2 HD. Ce BDNF réduit influence largement le déficit striatal associé à une déficience motrice et à la neuropathologie de la MH.
– Arribat Y, Talmat-Amar Y, Paucard A, Lesport P, Bonneaud N, Bauer C, Bec N, Parmentier ML, Benigno L, Larroque C, Maurel P, Maschat F. – Systemic delivery of P42 peptide: a new weapon to fight Huntington’s disease – Acta Neuropathol. Commun. 2014 Aug 5;2:86
– Marelli C and Maschat F. – The P42 peptide and Peptide-based therapies for Huntington’s disease Orphanet Journal of Rare Diseases (2016) 11:24
Le développement préclinique est en cours.
Une étude clinique de phase 1 / 2 devrait débuter au cours de l’année 2023.
Le produit possède une désignation Orphan Drug auprès de l’EMA et de la FDA
Cancer
Optimisation de la radiothérapie dans le traitement des cancers
La contrainte la plus importante liée à la radiothérapie vient du fait qu’en irradiant une tumeur, on ne peut pas éviter totalement d’irradier les tissus environnants.
Il y a donc un risque d’altération de cellules saines (c’est-à-dire non cancéreuses) situées à proximité de la zone qu’on souhaite traiter.
Les effets secondaires varient en fonction de la localisation de la tumeur irradiée.
Le NanoManganese protège les tissus sains irradiés et potentialise l’effet de la radiothérapie sur les cellules tumorales.
Une première étude pré clinique a montré cette double action, permettant d’envisager une véritable optimisation de l’efficacité de la radiothérapie dans le traitement des cancers.
Potentialisation des virus oncolitiques : une collaboration avec la société TRANSGENE
TRANSGENE (Euronext Paris : TNG), société de biotechnologie qui conçoit et développe des immunothérapies à base de virus contre les cancers et les maladies infectieuses, poursuit avec Medesis Pharma un accord de recherche collaborative avec options de licence exclusive afin de co-développer des inhibiteurs de l’expression des gènes dont la protéine intracellulaire diminue l’efficacité des virus oncolytiques. Cette collaboration permet de tester une approche innovante de modulation du microenvironnement tumoral, afin d’augmenter l’efficacité thérapeutique des virus oncolytiques.
Medesis Pharma réalise le design, la synthèse et la formulation de ces oligonucléotides dans la microémulsion Aonys. Transgene finance ces travaux et conduit les études pharmacologiques et mécanistiques.
AONYS® Technologie
Description de la technologie
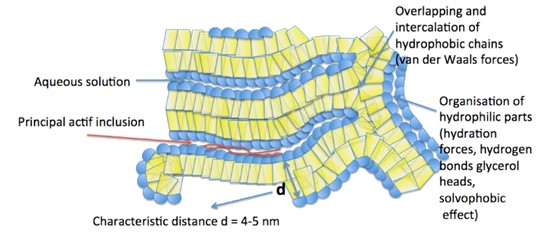
Administration buccale, transport invisible et protégé dans les Lipoprotéines HDL. Libération intracellulaire par les récepteurs SRB-1
Aonys est une technologie permettant la libération intracellulaire d’actifs pharmaceutiques hydrosolubles avec une administration buccale.

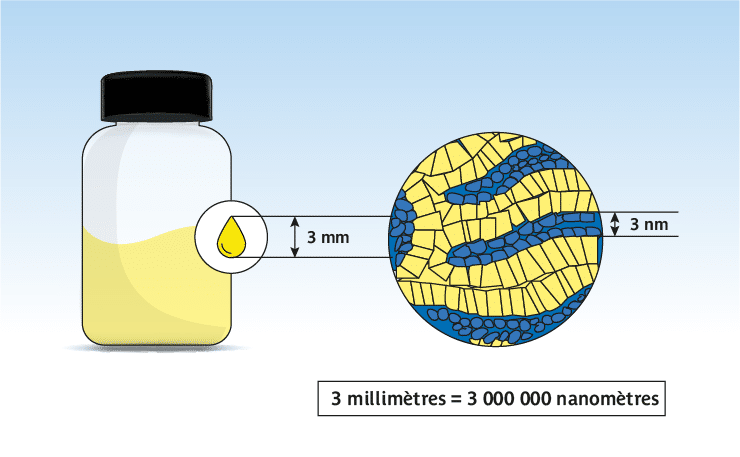
Aonys® est une microémulsion de micelles inverses (Water in Oil), qui est composée de deux phases : (1) une phase lipidique, (2) une phase aqueuse et un agent émulsifiant.
La phase lipidique est composée de :
- deux lipides pharmacopées : les mono-oléates de glycérol et les phytostérols,
- une lécithine permettant l’absorption à travers la muqueuse et la structuration en lipoprotéine HDL au contact des apoprotéines A1.
La phase aqueuse est une solution du principe actif dans l’eau.
Avantages de la technologie AONYS®
Administration buccale
Transport protégé et invisible
Délivrance intracellulaire par les récepteurs des lipoprotéines
Passage de la Barrière Hémato Encéphalique
Administration buccale
Contrary to popular belief, Lorem Ipsum is not simply random text. It has roots in a piece of classical Latin literature from 45 BC, making it over 2000 years old. Richard McClintock, a Latin professor at Hampden-Sydney College in Virginia, looked up one of the more obscure Latin words, consectetur, from a Lorem Ipsum passage, and going through the cites of the word in classical literature, discovered the undoubtable source. Lorem Ipsum comes from sections 1.10.32 and 1.10.33 of “de Finibus Bonorum et Malorum” (The Extremes of Good and Evil) by Cicero, written in 45 BC. This book is a treatise on the theory of ethics, very popular during the Renaissance. The first line of Lorem Ipsum, “Lorem ipsum dolor sit amet..”, comes from a line in section 1.10.32.
The standard chunk of Lorem Ipsum used since the 1500s is reproduced below for those interested. Sections 1.10.32 and 1.10.33 from “de Finibus Bonorum et Malorum” by Cicero are also reproduced in their exact original form, accompanied by English versions from the 1914 translation by H. Rackham.
Transport protégé et invisible
Contrary to popular belief, Lorem Ipsum is not simply random text. It has roots in a piece of classical Latin literature from 45 BC, making it over 2000 years old. Richard McClintock, a Latin professor at Hampden-Sydney College in Virginia, looked up one of the more obscure Latin words, consectetur, from a Lorem Ipsum passage, and going through the cites of the word in classical literature, discovered the undoubtable source. Lorem Ipsum comes from sections 1.10.32 and 1.10.33 of “de Finibus Bonorum et Malorum” (The Extremes of Good and Evil) by Cicero, written in 45 BC. This book is a treatise on the theory of ethics, very popular during the Renaissance. The first line of Lorem Ipsum, “Lorem ipsum dolor sit amet..”, comes from a line in section 1.10.32.
The standard chunk of Lorem Ipsum used since the 1500s is reproduced below for those interested. Sections 1.10.32 and 1.10.33 from “de Finibus Bonorum et Malorum” by Cicero are also reproduced in their exact original form, accompanied by English versions from the 1914 translation by H. Rackham.
Délivrance intracellulaire par les récepteurs des lipoprotéines
Contrary to popular belief, Lorem Ipsum is not simply random text. It has roots in a piece of classical Latin literature from 45 BC, making it over 2000 years old. Richard McClintock, a Latin professor at Hampden-Sydney College in Virginia, looked up one of the more obscure Latin words, consectetur, from a Lorem Ipsum passage, and going through the cites of the word in classical literature, discovered the undoubtable source. Lorem Ipsum comes from sections 1.10.32 and 1.10.33 of “de Finibus Bonorum et Malorum” (The Extremes of Good and Evil) by Cicero, written in 45 BC. This book is a treatise on the theory of ethics, very popular during the Renaissance. The first line of Lorem Ipsum, “Lorem ipsum dolor sit amet..”, comes from a line in section 1.10.32.
The standard chunk of Lorem Ipsum used since the 1500s is reproduced below for those interested. Sections 1.10.32 and 1.10.33 from “de Finibus Bonorum et Malorum” by Cicero are also reproduced in their exact original form, accompanied by English versions from the 1914 translation by H. Rackham.
Passage de la Barrière Hémato Encéphalique
Contrary to popular belief, Lorem Ipsum is not simply random text. It has roots in a piece of classical Latin literature from 45 BC, making it over 2000 years old. Richard McClintock, a Latin professor at Hampden-Sydney College in Virginia, looked up one of the more obscure Latin words, consectetur, from a Lorem Ipsum passage, and going through the cites of the word in classical literature, discovered the undoubtable source. Lorem Ipsum comes from sections 1.10.32 and 1.10.33 of “de Finibus Bonorum et Malorum” (The Extremes of Good and Evil) by Cicero, written in 45 BC. This book is a treatise on the theory of ethics, very popular during the Renaissance. The first line of Lorem Ipsum, “Lorem ipsum dolor sit amet..”, comes from a line in section 1.10.32.
The standard chunk of Lorem Ipsum used since the 1500s is reproduced below for those interested. Sections 1.10.32 and 1.10.33 from “de Finibus Bonorum et Malorum” by Cicero are also reproduced in their exact original form, accompanied by English versions from the 1914 translation by H. Rackham.
Histoire d’AONYS
Medesis Pharma SA a été créée en avril 2003 pour consolider et développer la propriété intellectuelle associée à la découverte de plusieurs composants lipidiques. Ces composants ont été identifiés dans une plante antidiabétique dont l’efficacité a été validée dans des modèles animaux en corrigeant les phénotypes associés à la résistance à l’insuline :
- 7 ans de screening avec des fractions purifiées extraites de urtica dioïca (plante médicinale méditerranéenne), testées sur 12 000 rats diabétiques.
- Identification de 3 lipides qui, lorsqu’ils sont associés à de très faibles concentrations de vanadium, ont démontré une activité thérapeutique chez des rats diabétiques.
- Évolution des fractions vers une formulation pharmaceutique.
- Optimisation de la technologie pour différents types de principes actifs.
Des recherches complémentaires ont permis le développement d’une formulation pharmaceutique, AONYS®, qui constitue la base de tous les produits dans le pipeline de recherche et de développement.
AONYS® et ses multiples applications sont protégées par 11 familles de brevets internationaux.